FIRENZE (ITALPRESS) – Risultati positivi dello Studio EMERALD su Elacestrant. Lo hanno annunciato il Gruppo Menarini e Radius Health Inc. al San Antonio Breast Cancer Symposium (SABCS). I dati sono stati presentati al congresso come "Late Breaker" e condivisi in una presentazione tenuta da Aditya Bardia, MD. EMERALD (NCT03778931) è uno studio di Fase III, multicentrico, internazionale, randomizzato, in aperto, con controllo attivo che ha valutato elacestrant somministrato in monoterapia verso lo SoC per il trattamento del carcinoma mammario avanzato/metastatico ER+/HER2-. Lo studio ha arruolato pazienti che avevano ricevuto 1 o 2 linee precedenti di terapia endocrina (ET). Criteri di eleggibilità obbligatori per tutti i pazienti erano la precedente progressione della malattia dopo trattamento con ET combinata con un inibitore di CDK4/6 e al massimo un ciclo di chemioterapia. Lo studio ha raggiunto entrambi gli endpoint primari dimostrando un prolungamento statisticamente e clinicamente significativo della sopravvivenza libera da progressione della malattia (Progression Free Survival- PFS) con elacestrant somministrato come monoterapia rispetto alla terapia endocrina standard (Standard of Care-SoC), sia nella popolazione complessiva che nel sottogruppo di pazienti con mutazione del recettore degli estrogeni (mESR1). Nella popolazione complessiva, elacestrant ha ridotto del 30% il rischio di progressione della malattia o di morte rispetto allo SoC. Nel sottogruppo di pazienti con mESR1, elacestrant ha ridotto del 45% il rischio di progressione della malattia o di morte rispetto allo SoC. Il tasso di PFS a 12 mesi è stato di 22.32% vs 9.42% rispettivamente con elacestrant vs SoC , e di 26.76% vs 8.19% nella popolazione con mESR1. Rispetto a fulvestrant, elacestrant ha dimostrato un prolungamento di PFS statisticamente significativo e ha ridotto il rischio di progressione di malattia o di morte del 32% nella popolazione generale e del 50% nel sottogruppo di pazienti mESR1. Alla luce di questi risultati, elacestrant diventa il primo SERD orale ad aver dimostrato in uno studio registrativo una maggiore efficacia rispetto a fulvestrant. Elacestrant è stato ben tollerato e ha il potenziale di diventare il nuovo standard di cura per questa popolazione di pazienti. Aditya Bardia, MD, oncologo presso il Mass General Cancer Center, Harvard Medical School e Principal Investigator dello studio EMERALD, ha commentato: "I pazienti con carcinoma mammario ER+/HER2- avanzato o metastatico già trattato hanno attualmente opzioni terapeutiche limitate a causa dello sviluppo della resistenza alla terapia endocrina da precedenti linee di trattamento". Bardia ha aggiunto: "Elacestrant – come primo SERD orale – ha il potenziale per diventare un nuovo standard di cura, visti i risultati ottenuti rispetto a fulvestrant (intramuscolare) e allo SoC nella popolazione generale e nel sottogruppo di pazienti ESR1. Nel prossimo futuro, elacestrant offrirà ai pazienti, alle loro famiglie e agli operatori sanitari un'opzione di trattamento efficace e sicura come monoterapia orale". Elcin Barker Ergun, Amministratore Delegato del Gruppo Menarini, ha commentato: "Siamo estremamente soddisfatti dei risultati dello studio EMERALD. I dati sembrano dimostrare che elacestrant può rappresentare un'alternativa orale ben tollerata ed efficace rispetto a fulvestrant e allo SoC in seconda/terza linea, per i pazienti affetti da carcinoma mammario avanzato o metastatico, compresi i pazienti il cui tumore presenta mutazioni ESR1 – uno dei sottogruppi più difficili da trattare in questo ambito. E' nostra intenzione sottomettere il dossier alle autorità regolatore negli Stati Uniti e nell'Unione Europea nel 2022 visti i risultati positivi di sicurezza ed efficacia e grazie a tutti i pazienti, le loro famiglie e gli operatori sanitari che hanno preso parte a questo importante studio clinico". Menarini prevede inoltre di avviare gli studi di combinazione e altre attività di ricerca in nuove linee di terapia, quali il setting adiuvante, consentendo un utilizzo più ampio di elacestrant per soddisfare i maggiori bisogni terapeutici per i pazienti con carcinoma mammario ER+/HER2-. Nel 2018 elacestrant ha ricevuto la designazione Fast Track da parte di FDA. (ITALPRESS). mgg/com 08-Dic-21 18:14
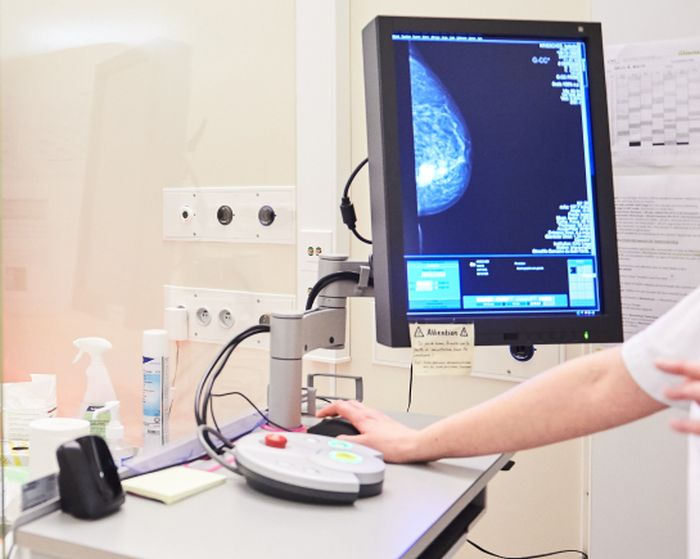
Carcinoma mammario, risultati positivi studio Emerald su Elacestrant
Redazione
“La Discussione” è una testata giornalistica italiana fondata nel 1953 da Alcide De Gasperi, uno dei padri fondatori dell’Italia moderna e leader di spicco nella storia politica del nostro paese.